Molecular Vectorology
Les vecteurs viraux AAV sont des outils de choix pour le transfert de gène in vivo. Leur efficacité n’est plus à prouver avec le succès de nombreux essais cliniques et la commercialisation de deux produits, Luxturna® et Zolgensma®. L’utilisation de ces nouveaux médicaments à haute dose, pour le traitement de maladies systémiques, pose pourtant de nouveaux défis dont le ciblage spécifique du tissu à traiter et le contournement de la réponse immune dirigé contre le vecteur. En effet, une réponse immune peut apparaitre contre la capside des vecteurs viraux AAV, l’ADN ou la protéine thérapeutique. Des impuretés ou des séquences étrangères présentent dans les lots de vecteurs peuvent également intervenir dans la détection du vecteur par le système immunitaire.
Notre équipe développe des méthodes analytiques pour caractériser les génomes AAVr par séquençage haut-débit (HTS) et étudie l’influence des séquences ADN sur l’efficacité des vecteurs viraux AAV.
Caractérisation des acides nucléiques par séquençage
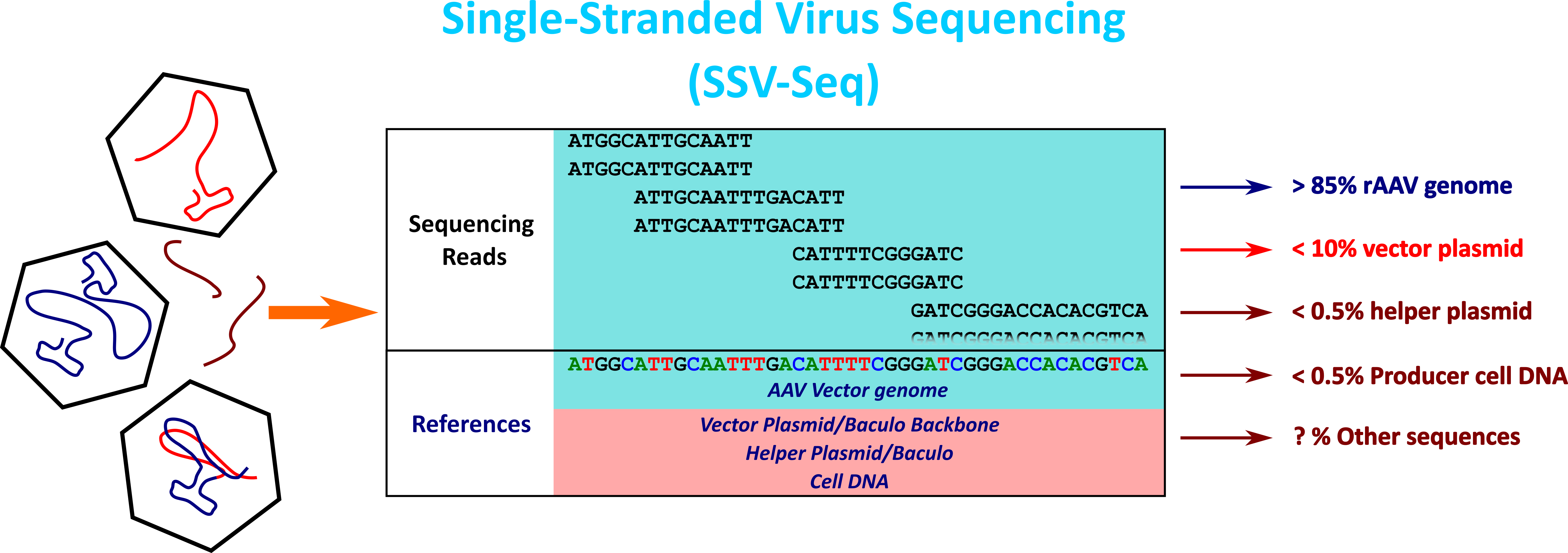
Nous avons développé une méthode basée sur le séquençage haut-débit (HTS) et un pipeline bio-informatique dédié pour analyser les ADN résiduels et l’identité des génomes AAVr. Cette méthode appelée SSV-Seq (Single-Stranded DNA Virus Sequencing) a été publiée (Lecomte et al. 2015, 2019).
La contamination des lots de vecteurs des ARN résiduels, en particulier par des microRNA cellulaires, est également étudiée car ils constituent un potentiel risque pour le patient.
Optimisation du genome vecteur AAVr
L’efficacité et la spécificité des vecteurs AAV dépendent de choix de la capside et également du design du génome AAVr (promoteur, éléments régulateurs…). Nos projets de recherche se focalise particulièrement sur le rôle des séquences terminales répétées (ITR), seules séquences virales présentes dans les vecteurs, lors du transfert de gène.

Membres de l'équipe
Magalie Penaud-Budloo, Ph.D., Senior scientistEmilie Lecomte, Bioinformatics scientist
Sylvie Saleun, Engineer
Marianne Laugel, PhD student