Next generation disease models – ATIP Avenir
L’objectif de l’équipe « Next generation disease models » est de développer de nouveaux modèles d’étude précliniques complémentaires aux expérimentations in vivo.
La thérapie génique utilisant des vecteurs viraux adéno-associés (AAV) est une approche prometteuse pour le traitement de nombreuses maladies, notamment d’origine génétique, qui peuvent toucher des tissus variés (muscles, foie, cerveau, rétine, etc.). Néanmoins, les modèles in vivo utilisés à ce jour ne permettent pas toujours de prédire leur efficacité thérapeutique ainsi que les effets secondaires parfois rencontrés chez les patients traités, ni de comprendre précisément certains mécanismes pathologiques subtils au niveau moléculaire. Le développement de thérapies géniques de deuxième génération va donc nécessiter de nouveaux modèles d’étude polyvalents, simples et rapides d’utilisation, et au plus proche des patients.
Notre équipe utilise les cellules souches induites à la pluripotence (cellules iPS) générées à partir de prélèvements de patient-e-s et différenciées en cellules d’intérêt organisées en deux dimensions ou en organoïdes tridimensionnels, dans le but de générer de nouveaux modèles in vitro de différentes maladies.
Nos activités s’articulent autour de deux axes majeurs :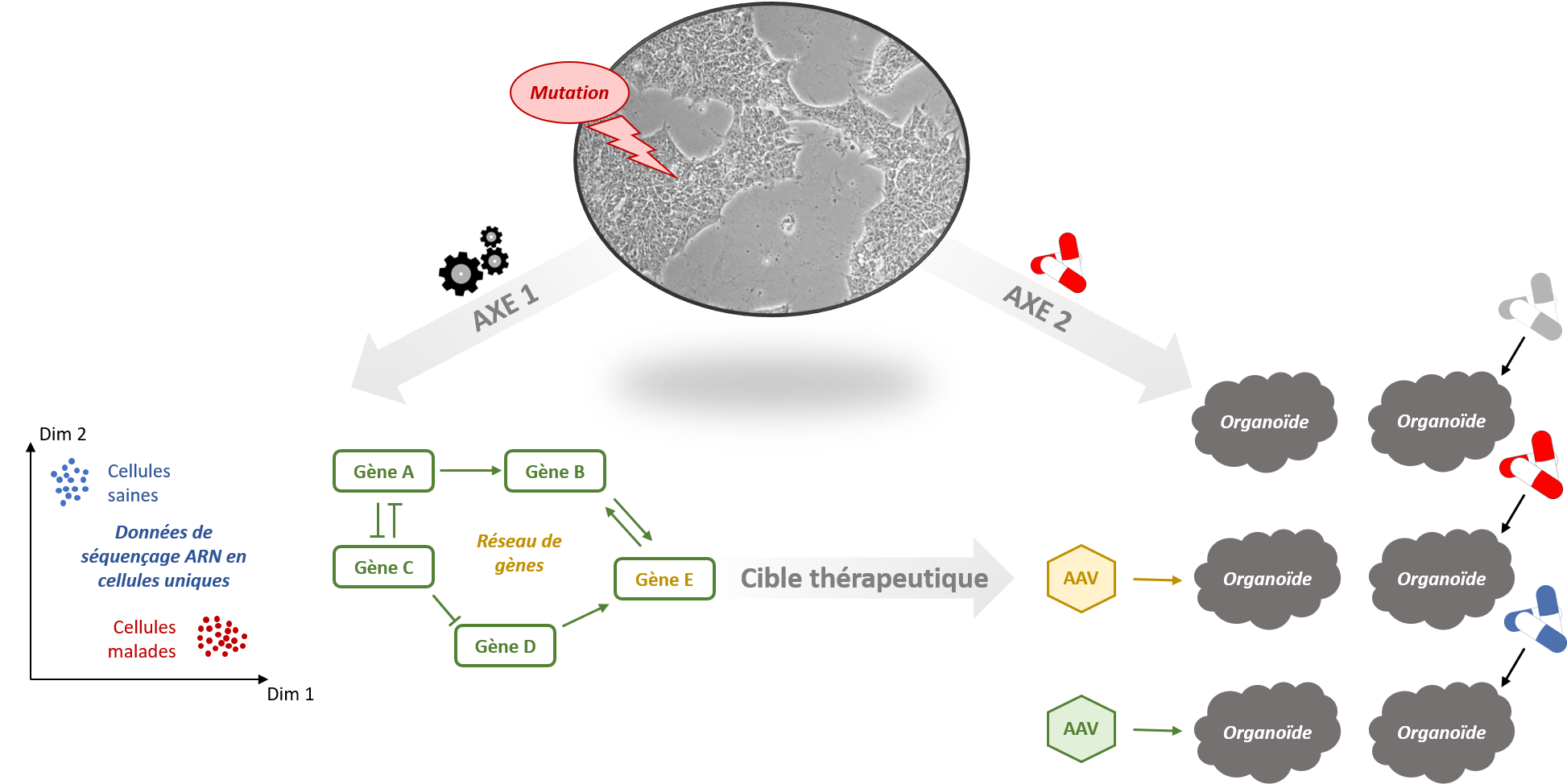
Identification de phénotypes précoces et de nouvelles cibles thérapeutiques
Dans ce premier axe, nous utilisons des lignées de cellules iPS porteuses de mutations spécifiques pour identifier leurs conséquences précoces lors du développement in vitro. Par des approches de séquençage de l’ARN sur cellules uniques (single-cell RNA-Seq) et des méthodes d’analyse bio-informatique de pointe, nous étudions la cinétique de différenciation des iPS et les réseaux de gènes dérégulés dans un contexte pathologique.
Développement préclinique sur organoïdes humains dérivés de cellules iPS de patients
Ce deuxième axe vise à proposer une plateforme de test préclinique in vitro basée sur des organoïdes humains dérivés de cellules iPS. Une telle plateforme permettra notamment de tester de nombreuses stratégies thérapeutiques en parallèle et en un temps record (thérapie génique AAV, pharmacologie, etc.). Pour ce faire, nous cherchons à mettre au point des protocoles de différenciation d’organoïdes robustes et reproductibles, permettant d’atteindre un niveau de maturation suffisant et mimant au plus près l’architecture tissulaire native.
Membres de l'équipe :
Jean-Baptiste Dupont, Ph.D, Team LeaderElise Mozin, Ingénieure d'étude
Anne-Maëlys Rannou, Etudiante M2
Clémence Lièvre, Etudiante M2, interne en pharmacie





